Definisi
Seperti yang telah dibahas pada pokok bahasan sebelumnya kita telah mengetahui bahwa kardiomiopati adalah penyakit atau kelainan otot jantung. Salah satu jenis kardiomiopati adalah kardiomiopati hipertrofik (KH) atau Hypertrophic Cardiomyopathy (HCM) dikenal juga sebagai idiopathic hypertrophic subaortic stenosis atau asymmetric septal hypertrophy didefinisikan sebagai hipertrofi dari miokardium dan penipisan septum interventrikular dibandingkan dengan dinding bebas dari ventrikel kiri (asimetris septal hipertrofi) dengan ukuran ruangan ventrikel kiri yang normal atau sedikit mengecil tanpa adanya hipertensi maupun stenosis aorta. Hal ini akan menyebabkan kelainan fungsional dari otot jantung. Kardiomiopati hipertrofik adalah suatu penyakit di mana terjadi hipertrofi (penebalan) dinding ventrikular secara berlebihan sehingga aliran darah keluar dari ventrikel kiri terhambat.
Kardiomiopati hipertrofik memiliki banyak nama lain seperti Teare's disease, Brock's disease, asymmetrical hypertrophic cardiomyopathy, hypertrophic obstructive cardio-miopathy, idiopathic hypertrophic cardiomyopathy, idiopathic hypertrophic subaortic stenosis, familial myocardial disease, namun demikian yang dipakai WHO adalah hypertrophic cardiomyopathy.
Kardiomiopati hipertrofik adalah penyakit primer dari
miokardium dimana sebagian dari miokardium mengalami hipertrofi (penebalan)
tanpa alasan pasti, yang mengakibatkan gangguan fungsional dari miokardium. Keadaan ini merupakan penyebab utama
dari kematian mendadak pada atlet berusia muda. Kejadian
kardiomiopati hipertrofik adalah penyebab signifikan dari kematian mendadak
pada kelompok umur manapun dan merupakan sebab dari gejala jantung yang sangat
mengganggu aktivitas. Orang yang berusia lebih muda lebih rentan untuk
terjadinya bentuk yang lebih parah dari kardiomiopati hipertrofi.
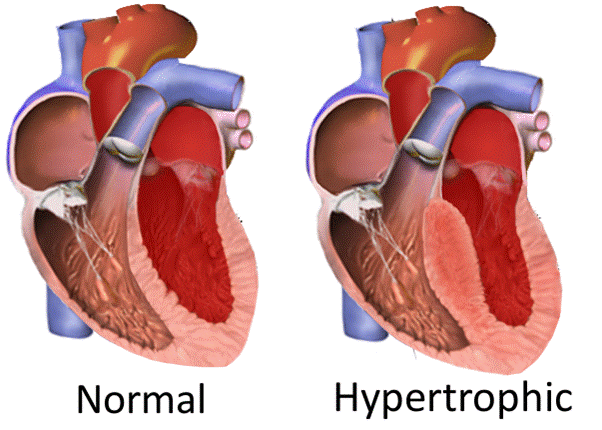 |
| Penampakan perbedaan kardiomiopati hipertrofik dengan jantung normal (dikutip dari wikipedia.org) |
HCM terkadang asimtomatik (tidak menunjukkan gejala)
sampai terjadinya kematian jantung mendadak, sehingga dikarenakan alasan ini,
beberapa pihak menyarankan pemeriksaan screening
rutin pada populasi tertentu untuk
mendeteksi penyakit ini.
Pada KH (kardiomiopati hipertrofik), miosit (sel kontraktil jantung) di jantung
meningkat dalam ukuran, yang mengakibatkan penebalan otot jantung. Selain itu,
garis barisan otot jantung juga mengalami perubahan, fenomena ini dikenal myocardial
disarray. HCM juga menyebabkan gangguan fungsi kelistrikan pada jantung. HCM
paling umum disebabkan oleh mutasi pada salah satu dari sembilan gen sarcomeric
yang mengakibatkan protein yang termutasi pada sarkomer, yang adalah komponen
utama dari miosit (sel otot jantung). Hal ini kebanyakan adalah mutasi missense
titik tunggal pada rantai berat beta-myosin heavy (MHC), myosin-binding protein
C, cardiac troponinT, atau tropomyosin. Mutasi ini menyebabkan kelainan
struktural miofibril dan miosit dan kemungkinan defisiensi dalam menghasilkan
kekuatan.
Walaupun beberapa
literatur sementara ini fokus pada populasi Eropa, America, dan Jepang,
HCM dapt terjadi pada semua kelompok etnis. Prevalensi HCM adalah sekitar 0.2%
sampai dengan 0.5% dari populasi umum.
Kardiomiopati hipertrofik didapatkan di seluruh dunia,
kejadian kurang lebih sama antara pria dan wanita, tetapi berbeda pada etnis
atau ras tertentu (banyak pada orang Jepang), paling banyak pada orang muda usia 20-30
tahun, namun bervariasi dari 6 bulan sampai lebih 60 tahun. Pada populasi umum
diperkirakan prevalensinya 1 : 500. Terdapat dua fitur utama dari KH yaitu (1) hipertrofi
ventrikel kiri yang asimetris, seringkali terdapat pada septum
interventrikular, (2) tekanan aliran ventrikel kiri yang dinamis, yang
berhubungan dengan menyempitnya area subaorta sebagai konsekuensi dari
midsistolik apposition dari katup mitral anterior melawan septum yang hipertrofi.
Contohnya systolic anterior motion (SAM) dari katup mitral.
Patofisiologis abnormalitasnya tidak pada sistolik namun pada fungsi diastolik,
dengan karakteristik meningkatnya kekakuan pada otot jantung yang mengalami hipertrofi.
Hal ini mengakibatkan meningkatnya tekanan pengisian diastolik. Pola hipertrofi
dari KH berbeda dengan yang terlihat pada hipertrofi sekunder (misalnya
hipertensi). Kebanyakan pasien mempunyai variasi pada ketebalan septum
ventrikel yang tidak proporsional ketika dibandingkan dengan dinding yang
bebas. Pasien lainnya mungkin memperlihatkan disproporsi dari apex atau dinding
bebas ventrikel kiri, dan hanya 10% pasien yang memiliki keterlibatan
konsentris dari ventrikel. Pada beberapa anak, kompresi sistolik segmen
intramiokardial dari arteri koroner dapat mengakibatkan iskemia dan kematian. Kardiomiopati
hipertrofik ini ditandai dengan adanya penebalan pada dinding ventrikel tanpa
dilatasi, pada kebanyakan kasus ini menyebabkan gagal jantung. Penyakit ini
diturunkan secara genetik (dominant autosomal) dan diduga juga disebabkan karena
rangsangan katekolamin, kelainan pembuluh darah koroner kecil, kelainan yang
menyebabkan iskemi miokard, serta kelainan konduksi atrioventrikuler. Ada 2 macam
kardiomiopati hipertrofik yaitu : (1) hipertrofi yang simetris atau konsentris dan (2) hipertrofi septal
asimetris.
Obstructif dan non-obstruktif
Berdasarkan
pada apakah distorsi anatomi jantung
menyebabkan obstruksi atau tidak dari aliran keluar darah pada ventrikel kiri,
HCM dapat dibagi menjadi obstruktif atau tidak obstruktif.
- Jenis obstruktif dari HCM, hypertrophic obstructive cardiomyopathy
(HOCM) juga dikenal dengan nama idiopathic
hypertrophic subaortic stenosis (IHSS) dan asymmetric septal hypertrophy (ASH).
- Jenis non obstruktif dari HCM
adalah apical hypertrophic
cardiomyopathy, juga dikenal sebagai Yamaguchi Syndrome
atau Yamaguchi Hypertrophy, istilah
ini pertama kali digunakan pada individu keturunan Jepang.
Epidemiologi
Hypertrophic
cardiomyopathy (HCM) dilaporkan ada pada
0.5% pasien rawat jalan yang dirujuk untuk dilakukan ekokardiografi.
Prevalensi keseluruhan HCM rendah dan diperkirakan terjadi pada 0.05-0.2% dari populasi. Bukti
morfologis dari penyakit ini ditemukan oleh ekokardiografi pada sekitar 25%
kerabat / saudara derajat pertama dari pasien dengan HCM. Pemeriksaan genetis
masih sedang dalam tahap awal perkembangan penelitian namun sudah dapat digunakan untuk
mengidentifikasi anggota keluarga asimtomatis dengan mutasi yang sama dengan proband (index kasus).
Demografi berdasarkan jenis kelamin
HCM sedikit lebih sering terjadi pada laki-laki dibanding
perempuan. Namun demikian, pola genetik yang diturunkan adalah dominan
autosomal, tanpa predileksi jenis kelamin. Modifikasi faktor genetis, hormonal
dan lingkungan dapat menyebabkan kemungkinan identifikasi yang lebih mengarah
pada laki-laki, peningkatan simtomatologi, atau derajat obstruksi aliran keluar
ventrikel kiri yang lebih besar, dengan temuan yang lebih menonjol pada
pemeriksaan fisik.
HCM biasanya terjadi pada usia lebih muda pada perempuan.
Perempuan lebih cenderung simtomatis dan lebih terganggu aktivitasnya karena
gejala yang ditimbulkan dibanding dengan laki-laki.
Demografi berdasarkan usia
Secara umum, kejadian usia HCM adalah kurva bimodal. Kejadian
yang paling umum adalah pada usia dekade ketiga, namun dapat terjadi pada usia
berapa saja, dari bayi baru lahir, sampai usia lanjut.
Pada kasus yang diturunkan, dapat ditemukan pada rentang
usia baru lahir hingga dewasa, dengan kejadian paling umum adalah pada umur
dekade kedua. Pada dewasa yang tidak diturunkan, kejadian paling umum adalah
umur dekade ketiga, dengan variasi kasus terjadi antara usia dekade ketiga
hingga keenam.
Etiologi
Penyebab kardiomiopati hipertrofik
tidak diketahui secara pasti, diduga disebabkan oleh kelainan faktor genetik,
familial, rangsangan katekolamin, kelainan pembuluh darah koroner kecil,
kelainan yang menyebabkan iskemi miokard, kelainan konduksi atrioventrikuler
dan kelainan kolagen.
Kemajuan bidang biomolekuler
mengungkapkan adanya mutasi gen yang mengatur protein sarkomer jantung,
setengah dari pasien kardiomiopati hipertrofik mempunyai riwayat keluarga
positif dengan transmisi autosomal dominan. Lebih dari 150 mutasi telah
diketahui dari 10 lokasi yang berbeda yang mengkode protein sarkomer. Sekitar
40% dari mutasi ini berhubungan dengan gen B dari heavy chain cardiac myosin yang berada pada kromosom 14q11, 1q3,
15q2 dan 11p13-q13, dimana mesenger RNA
dapat dikenali dari limfosit perifer dari PCR,
sehingga kelainan ini dapat dideteksi sebelum adanya kelainan klinis yang
nyata.2,8,9 Sekitar 15% mempunyai mutasi dari gen troponin T cardiac (kromosom 11), 10 %
mutasi pada myosin binding protein C,
5% mutasi pada gen alfa tropomyosin.
Kardiomiopati jenis ini ada dua kategori penebalan
miokardium, yaitu:
- Asimetrik septal kardiomiopati hipertrofik (subaortic stenosis)
- Hipertensi atau valvular kardiomiopati hipertrofik.
Kedua
jenis kardiomioapti hipertrofik ini berbeda pada etiologi, patofisiologi, dan
manifestasi klinisnya.
HCM jenis pertama yang juga dikenal
sebagai “idiopatik HCM” merupakan penyakit autosomal dominan yang mengakibatkan
penebalan dari dinding septum, sehingga terjadi obstruksi aliran menuju ventrikel
kiri. HCM jenis ini disebabkan oleh mutasi protein kontraktil dari sarkomer
jantung. Sekarang ini, 11 gen mutan berhubungan dengan HCM, terutama B-myosin
rantai berat (yang pertama dikenali) dan protein pengikat miosin. Perubahan
lain yang terjadi yaitu deposit abnormal dari kolagen dan penurunan protein
kontraktil pada miosit.
Penebalan dinding septum
mengakibatkan terjadinya keadaan hiperdinamik terutama saat beraktivitas.
Relaksasi diastolik juga terganggu dan kemampuan ventrikel untuk mengembang
menurun. Obstruksi aliran ventrikel kiri dapat muncul apabila detak jantung
meningkat dan volume intravaskular menurun. Gejala yang dapat muncul seperti
angina, sinkop, palpitasi, dan tanda-tanda infark miokard serta gagal jantung
kiri.
Meskipun pada umumnya pasien dapat
asimtomatis, namun dyspnoe merupakan keluhan yang sering didapatkan, hampir
pada 90% pasien yang simtomatis. Dyspnoe muncul sebagai akibat kekakuan,
ventrikel yang tak mampu mengembang, sehingga mengakibatkan meningkatnya
tekanan end-diastolik ventrikel kiri serta relaksasi abnormal ventrikel.
HCM
jenis kedua akan muncul apabila terjadi peningkatan resistensi ejeksi ventrikel
yang biasanya ditemukan pada keadaan hipertensi atau stenosis katup (biasanya
aorta). Dalam hal ini, hipertrofi dari miosit merupakan kompensasi untuk
meningkatkan workload, sehingga apabila terjadi disfungsi miosit yang
berkepanjangan dapat mengakibatkan disfungsi diastolik dan akhirnya dapat
menyebabkan disfungsi sistolik dari ventrikel.
Kinetik
kalsium yang abnormal
Data menunjukkan hubungan kinetik
kalsium miokardial sebagai penyebab hipertrofi miokardial irreguler dan fitur
tertentu dari HCM, khususnya pada pasien dengan kelainan fungsional diastolik.
Kinetik kalsium miokardial yang abnormal dan aliran kalsium abnormal dari
peningkatan jumlah saluran kalsium mengakibatkan meningkatnya konsentrasi
kalsium intraseluler, yang mana pada akhirnya dapat menghasilkan hipertrofi dan
ketidakteraturan cellular.
Penyebab
genetik
HCM familial terjadi sebagai penyakit
Mendelian-inherited dominan autosomal
pada sekitar 50% kasus. Beberapa, atau sedikit sekali, terjadi karena
pembentukan sporadis dari penyakit ini yang diakibatkan mutasi spontan.
Setidaknya ada 6 gen berbeda pada
paling sedikit 4 kromosom yang diasosiasikan dengan HCM, dengan lebih dari 50
mutasi yang berbeda yang ditemukan sejauh ini. HCM familial adalah penyakit
yang secara genetik heterogen yang maksudnya adalah dapat disebabkan defek
genetik pada lebih dari 1 locus.
Pada tahun 1989, Seidman et al
pertama kali melaporkan dasar genetik untuk HCM. Mereka melaporkan adanya suatu
gen penyakit yang berlokasi pada lengan panjang kromosom 14. Kemudian
selanjutnya, mereka menemukan bahwa ini merupakan gen yang mengkode rantai
berat beta myosin kardiak.
Sekitar 50-60% pasien dengan indeks tinggi kecurigaan
klinis akan adanya HCM akan
teridentifikasi mutasi pada setidaknya 1 dari 9 gen sarcomeric. Sekitar 45%
dari mutasi ini terjadi pada gen rantai berat myosin beta pada kromosom 14
q11.2-3, sementara sekitar 35% terlibat dengan gen protein C kardiak yang
mengikat myosin. Dikarenakan HCM umumnya adalah bersifat dominan autosomal,
anak dengan salah satu orangtua menderita HCM memiliki 50% kemungkinan
menurunkan mutasi yang menyebabkan penyakit ini. Ketika sebuah mutasi
diidentifikasi melalui pemeriksaan
genetik, pemeriksaan genetik spesifik keluarga dapat digunakan untuk
mengidentifikasi kerabat yang berisiko terhadap penyakit ini.
Pada individu tanpa riwayat keluarga
HCM, penyebab paling umum penyakit ini adalah mutasi de novo dari gen yang memproduksi rantai berat beta myosin.
Sebuah polimorfisme insertion/deletion pada gen yang
mengkode angiotensin converting enzyme (ACE) merubah fenotip dari penyakit
ini. Genotip D/D (deletion/deletion)
dari ACE diasosiasikan dengan hipertrofi tertanda dari ventrikel kiri dan
mungkin berhubungan dengan risiko lebih tinggi akan prognosis yang tidak baik.
Beberapa mutasi dapat memiliki
potensial yang lebih buruk dari yang lain (Rantai berat β myosin). Contohnya,
mutasi troponin T pada mulanya diasosiasikan dengan 50% angka kematian sebelum
usia 40. Selain itu, sebuah penelitian
baru dan lebih besar menemukan risiko yang serupa pada mutasi protein sarkomer
lainnya.
Variasi yang beragam ada dalam
ekspresi fenotipik dari mutasi tertentu pada gen tertentu, dengan keberagaman
dalam gejala klinis dan hipertrofi yang terjadi. Keberagaman fenotipik
berhubungan dengan perbedaan dalam genotip, dengan mutasi spesifik dikaitkan
dengan gejala tertentu, derajat hipertrofi, dan prognosis.
Kemungkinan penyebab lain
Penyebab
lain yang dimungkinkan dari HCM antara lain :
- Stimulasi
saraf simpatis yang abnormal – Peningkatan responsivitas jantung terhadap
produksi katekolamin yang berlebihan atau penurunan uptake neuronal dari norepinephrine dapat menyebabkan HCM.
- Arteri
koroner intramural yang menebal secara abnormal – arteri ini tidak
berdilatasi secara normal, yang
akan mengarah ke iskemia miokard, kemudian berkembang menjadi fibrosis miokard dan hipertrofi
kompensasi abnormal
- Iskemia
subendokardial – Hal ini berhubungan dengan abnormalitas mikrosirkulasi
jantung yang menghabiskan cadangan energi essensial untuk pengolahan
konsumsi kalsium selama diastol; iskemia subendokardial mengakibatkan
interaksi persisten dari elemen kontraktil selama diastol dan peningkatan
kekakuan diastolik.
- Abnormalitas struktural jantung Cardiac – Yang termasuk di dalamnya adalah konfigurasi bentuk catenoid dari septum, yang mengakibatkan hipertrofi dan ketidakteraturan sel miokardial.
Pada penyakit kardiomiopati hipertrofik ini didapati hipertrofi
ventrikel yang masif terutama pada septum ventrikel yang mengakibatkan pada
waktu sistole septum menonjol ke aliran keluar ventrikel kiri dan menyebabkan
obstruksi. Adakalanya ventrikel kanan dapat terkena. Beberapa tingkatan
fibrosis miokard dapat dijumpai. Katup mitral bergeser ke anterior karena
hipertrofi muskulus papilaris dan ruang ventikel kiri diisi oleh hipertrofi
yang masif. Kelainan hemodinamik yang terjadi akibat hipertrofi, fibrosis, dan
kekakuan otot jantung berupa menurunnya distensibilitas jantung, sehingga
terjadi resistensi dalam pengisian ventrikel kiri, tetapi fungsi pompa
diastolik tetap normal sampai akhir penyakit. Obstruksi aliran ventrikel kiri
dapat berkembang karena kelainan letak daun anterior katup mitral yang
berhadapan dengan septum yang hipertrofi dan peak systolik pressure gradient pada aliran keluar ventrikel kiri
bervariasi. Berbeda dengan obstruksi yang disebabkan oleh orifisium yang
menyempit secara permanen, seperti pada stenosis aorta, pada kardiomiopati
hipertrofi, obstruksi jalur keluar ventrikel kiri merupakan hal yang dinamis
dan dapat berubah di antara pemeriksaan. Obstruksi muncul dari hasil
penyempitan aliran ventrikel kiri yang telah kecil sebelumnya oleh SAM dari katup mitral terhadap septum
yang hipertrofi dan kontak midsistolik dengan septum ventrikel. Delapan puluh
persen pasien dengan karrdiomiopati hipertrofik mengalami gangguan diastolik
yaitu kelainan dalam relaksasi dan pengisian ventrikel. Sebaliknya fungsi
sistolik normal sampai super-normal. Kebanyakan pasien memiliki fraksi ejeksi
supernormal (75-80%).
Sejak pertama kali HCM dipelajari, fitur yang menarik
perhatian cukup besar adalah gradien tekanan dinamis yang melintasi traktus
(jalur) outflow (aliran keluar)
ventrikel kiri. Gradien tekanan tampaknya berhubungan dengan penyempitan lebih
lanjut dari jalur outflow yang sudah kecil (sebelumnya sudah menyempit karena
hipertrofi septal asimetris dan kemungkinan lokasi abnormal katup mitral) yang
disebabkan systolic anterior motion (SAM)
dari katup mitral terhadap septum yang telah mengalami hipertrofi.
Tiga penjelasan kemungkinan sebab terjadinya SAM dari
katup mitral telah dikemukakan, sebagai berikut: (1) Katup mitral ditarik
terhadap septum oleh kontraksi muskulus papillaris, yang terjadi karena lokasi
abnormal katup dan hipertrofi septum yang mengubah orientasi muskulus
papillaris tersebut; (2) Katup mitral terdorong terhadap septum karena posisi
abnormalnya pada outflow tract; (3) Katup
mitral mendekat terhadap septum karena tekanan rendah yang terjadi pada saat
darah diejeksi pada kecepatan tinggi melalui jalur aliran keluar (outflow tract) yang menyempit (efek Venturi) .
Kebanyakan pasien dengan HCM memiliki fungsi diastolik
abnormal (baik ditemukan atau tidaknya tekanan gradien), yang kemudian akan
mengganggu pengisian ventrikel dan meningkatkan tekanan pengisian, walaupun
kavitas ventrikel berukuran kecil atau normal. Pasien ini memiliki kinetik
kalsium yang abnormal dan iskemia seubendokardial, yang berkaitan dengan
hipertrofi yang mencolok dan proses myopathic.
Individu dengan HCM memiliki derajat hipertrofi ventrikel
kiri yang berbeda-beda. Biasanya ini adalah hipertrofi asimetris, yang
melibatkan septum interventrikular, dan dikenal sebagai hipertrofi septal
asimetris. Ini merupakan kebalikan dari hipertrofi konsentris yang ditemukan
pada stenosis aorta dan hipertensi. Sekitar dua per tiga individu dengan HCM
memiliki hipertrofi septal asimetris.
Sekitar 25% individu dengan HCM menunjukkan suatu
obstruksi terhadap aliran keluar darah dari ventrikel kiri pada saat istirahat.
Meski demikian pada sebanyak 70% pasien, obstruksi dapat diprovokasi oleh
kondisi tertentu. Ini dikenal sebagai obstruksi aliran keluar dinamis (dynamic outflow obstruction), karena
derajat obstruksi bervariasi dan tergantung pada kondisi loading (Pengisian ventrikel dan tekanan darah arterial) dan
keadaan kontraktilitas dari ventrikel kiri.
Hipertrofi miokardial dan fibrosis ekstraselluler dapat
mempredisposisi peningkatan kekakuan ventrikel kiri yang bersamaan dengan
energetika cellular yang terkompromi dan penanganan kalsium yang abnormal
mengakibatkan disfungsi diastolik yang bermanifestasi sebagai dyspnea dan intoleransi terhadap latihan / olahraga.
Perubahan struktur pembuluh koroner dan peningkatan
tekanan diastolik (penurunan supply
darah) bersamaan dengan hipertrofi dan obstruksi outflow tract (peningkatan permintaan / demand) menyebabkan iskemia
miokard yang bermanifestasi sebagai angina
dan dapat bertanggungjawab memicu aritmia
ventrikuler.
Pada sekitar 30% pasien terdapat respons vaskular
abnormal dan ketidakmampuan untuk meningkatkan tekanan darah sistolik pada saat
latihan. Hal ini salah satunya disebabkan oleh reflek inhibisi kardiak secara
berlebihan yang diinisiasi oleh
peningkatan stress dinding miokardial dan kenaikan kadar unsur yang menyebabkan
vasodilatasi (peptida natriuretik).
Obstruksi outflow dinamis
Obstruksi ini (ketika ditemukan pad HCM) biasanya
dikarenakan oleh SAM dari daun katup anterior dari katup mitral. SAM (Systolic anterior motion) pada awalnya
diduga dikarenakan tonjolan septal subaorta, yang menyempitkan jalur aliran
keluar, menyebabkan aliran berkecepatan tinggi dan efek Venturi (sebuah tekanan
dibawah normal yang lokal pada jalur aliran keluar-outflow tract) . Tekanan yang rendah diduga menghisap katup mitral
ke arah anterior menuju septum. Tetapi SAM setelah diobservasi adalah suatu
fenomena kecepatan rendah. SAM mulai dari kecepatan (velocity) tidak berbeda
dengan yang diukur pada jantung yang normal. Sehingga, besarnya pengaruh dan
pentingnya gaya Venturi pada outflow tract ternyata tidak sebesar
yang diduga sebelumnya, dan gaya Venturi bukanlah gaya (force) utama yang
menyebabkan SAM.
Bukti ekokardiografik terbaru mengindikasikan adanya suatu
drag, gaya mendorong oleh aliran yang
merupakan gaya (force) hidrodinamik dominan pada daun katup mitral. Pada HCM
obstruktif, daun katup mitral seringkali berukuran besar dan memiliki posisi
lebih anterior pada kavitas ventrikel kiri dikarenakan posisi musculi
papillaris yang berada di posisi aanterior, yang pada saat pembedahan
seringkali “menempel” pada dinding anterior ventrikel kiri dengan perlekatan
yang abnormal.
Tonjolan mid-septal memicu malposisi katup dan
mengalihkan arah aliran keluar sehingga akan datang dari arah lateral dan
posterior. Arah aliran keluar (outflow)
yang abnormal dapat divisualisasikan di belakang dan lateral dari katup mitral
yang membesar, dimana dia akan ditangkap dan kemudian mendorongnya ke septum.
Ada suatu tumpang-tindih antara porsi aliran masuk dan aliran keluar pada
ventrikel kiri. Seiring perkembangan SAM pada awal sistol sudut antara outflow dan daun katup mitral yang
menonjol semakin membesar. Sebuah area permukaan yang meluas dari daun katup
kini terekspose terhadap drag
sehingga tambah memperkuat gaya pada daun katup – drag meningkat dengan peningkatan relatif sudut terhadap aliran. Analoginya adalah sebuah pintu terbuka pada
koridor yang sedang bertiup angin : pintu mulai bergerak secara perlahan dan
kemudian meningkat kecepatannya seiring dengan terpaparnya area permukaan yang
lebih luas terhadap angin sehingga akhirnya pintu menutup dengan kencang. Syarat kondisi yang diperlukan untuk
mempredisposisi SAM adalah : posisi katup mitral di anterior pada ventrikel
kiri, geometri ventrikel kiri yang berubah sedemikian rupa sehingga dapat
mengakibatkan aliran untuk mengarah ke katup mitral dari arah belakang, dan
pemendekan dan kekakuan chordae (chordal
slack). SAM dapat dianggap sebagai prolaps mitral yang diarahkan secara
anterior. Pada kedua kondisi tersebut katup mitral membesar dan berubah posisi
pada sistol oleh gaya dari aliran dan mengakibatkan regurgitasi mitral.
Dikarenakan katup mitral baru akan ditarik ke dalam jalur
aliran keluar ventrikel kiri / left
ventricular outflow tract (LVOT) hanya setelah katup aorta membuka, upstroke awal dari nadi arterial akan
normal. Ketika daun katup mitral terdorong kedalam LVOT, denyut arterial
sementara akan kolaps dan kemudian
diikuti oleh kenaikan kedua, bersamaan dengan saat tekanan ventrikel
kiri mengatasi obstruksi yang meningkat
yang disebabkan oleh SAM dari katup mitral. Ini dapat terlihat pada saat
pemeriksaan fisik sebagai ketukan ganda pada palpasi impuls apikal dan sebagai
pulsasi ganda pada palpasi nadi karotid, yang dikenal sebagai bifid pulse.
Gejala kardiomiopati hipertrofik (HCM) dapat termasuk
diantaranya adalah can include dyspnea, angina, orthopnea, syncope dan
presyncope, palpitasi, orthopnea,
paroxysmal nocturnal dyspnea, gagal jantung kongestif, nyeri kepala, dan
kematian jantung mendadak.
Kematian jantung mendadak
Ini merupakan manifestasi paling merugikan dan berbahaya
dari HCM. Insidensi tertinggi terjadi pada anak usia pra-remaja dan remaja dan
biasanya berkaitan dengan aktivitas kegiatan yang sangat membutuhkan tenaga
berat. Risiko kematian mendadak pada anak dapat
setinggi 6 % setiap tahun.
Pada lebih dari 80% kasus, aritmia yang menyebabkan
kematian mendadak adalah fibrilasi ventrikular. Pada banyak kasus ini
perburukan menjadi fibrilasi ventrikular berasal dari aritmia atrial cepat (rapid atrial arrhythmias), seperti
fibrilasi, takikardia supreventrikular, atau sindrom Wolff-Parkinson-White, sementara
yang lain berasal dari takikardia ventrikular dan kolaps hemodinamik dengan cardiac output yang rendah.
Dyspnea
Ini merupakan gejala yang paling umum muncul, terjadi
pada sebanyak 90% pasien simtomatik. Dyspnea secara garis besar adalah
konsekuensi dari peningkatan tekanan pengisian diastolik ventrikel kiri (dan
penjalaran peningkatan tekanan tersebut terhadap sirkulasi pulmonal).
Peningkatan tekanan pengisian ventrikel kiri pada prinsipnya disebabkan oleh
gangguan fungsi diastolik sebagai akibat dari hipertofi ventrikel.
Syncope
Syncope adalah gejala yang cukup umum, yang berasal dari
ketidakcukupan cardiac output pada
saat aktivitas berat atau dari aritmia kardiak. Lebih umum terjadi pada anak
dan dewasa muda dengan ukuran bilik ventrikel kiri yang lebih kecil dan bukti
ditemukannya takikardia ventrikel pada saat pengawasan yang berjalan.
Penyebab lain syncope adalah langsung dari aritmia, baik
dari takkardia maupun bradikardia. Beberapa pasien dengan HCM memiliki
abnormalitas dalam fungsi sinus node, yang akhirnya mengarah ke sindrom sinus
dengan terjadinya secara bergantian takiaritmia dan bradiaritmia atau bradiaritmia
parah.
Syncope
(sinkop) dan presyncope menjadi penanda risiko tinggi akan kematian mendadak
dan menjadi indikasi penanganan segera
pengobatan yang agresif.
Presyncope
Presyncope
termasuk didalamnya adalah gejala "graying-out" (penderita
berangsur-angsur secara perlahan kehilangan kesadaran dengan pandangan berkabut
keabu-abuan) pada keadaan berdiri dan membaik pada posisi berbaring. Hal ini
dapat berlangsung secara umum dan menjadi penanda akan risiko tinggi kematian
mendadak. Gejala ini dapat dieksaserbasi oleh stimulasi vagal. Presyncope juga
dapat terjadi pada takiaritmia atrial maupun ventrikular yang unsustained.
Angina
Gejala angina cukup umum pada pasien dengan HCM dan dapat
terjadi pada ketiadaan aterosklerosis koroner yang terdeteksi. Relaksasi
diastolik yang terganggu dan konsumsi oksigen miokardial yang meningkat
disebabkan oleh hipertrofi ventrikular yang mengakibatkan iskemia
subendokardial, terutama pada saat aktivitas berat.
Palpitasi
Palpitasi juga cukup umum pada penderita penyakit ini.
Hal ini merupakan akibat dari aritmia seperti detak atrial dan ventrikel
prematur, jeda sinus, fibrilasi atrial, atrial flutter, takikardia
supraventrikular, dan takikardia ventrikular.
Orthopnea dan paroxysmal nocturnal dyspnea
Hal ini merupakan tanda awal gagal jantung kongestif dan,
meskipun relatif jarang, ditemukan pada pasien dengan HCM parah. Hal ini adalah
akibat dari fungsi diastolik terganggu dan peningkatan tekanan pengisian
ventrikel kiri. Orthopnea dan paroxysmal nocturnal dyspnea adalah hasil dari
kongesti vena pulmonal.
Gagal Jantung Kongestif
Hal
ini relatif jarang tapi diawasi pada pasien dengan HCM parah. Keadaan ini dapat
diakibatkan oleh kombinasi gangguan fungsi diastolik dengan iskemia
subendokardial. Fungsi sistolik pada pasien ini hampir selalu terjaga baik.
Pusing berputar
Pusing kepala umum ditemukan pada pasien HCM dengan
peningkatan tekanan gradien yang melintas pada traktus aliran keluar ventrikel
kiri. Keadaan ini diperburuk oleh aktivitas berat dan dapat dieksaserbasi oleh
hipovolemia yang mengikuti aktivitas berat atau kehilangan cairan yang tidak
disadari (seperti pada suhu panas yang ekstrim).
Pusing juga dapat terjadi karena pergerakan, seperti
berdiri mendadak atau valsava pada saat buang air besar, atau pengobatan
tertentu, seperti diuretik, nitrogliserin, agen antihipertensi vasodilatasi,
yang menurunkan preload dan afterload dan meningkatkan tekanan
gradien yang melintas pada traktus aliran keluar ventrikel kiri.
Pusing juga dapat disebabkan hipotensi yang berhubungan
dengan aritmia dan penurunan perfusi serebral. Aritmia nonsustained sering menyebabkan gejala pusing kepala, kepala yang
terasa ringan, dan presinkop, dimana aritmia sustained lebih cenderung mengakibatkan sinkop, kolaps, dan / atau
kematian jantung mendadak.
Pemeriksaan fisik
Adanya dua impuls apikal
adalah akibat dari kontraksi atrial kiri yang sangat kuat terhadap
ventrikel kiri yang sangat menurun fungsinya. Ini cukup umum terjadi pada
pasien dewasa. Tiga impuls apikal
disebabkan tonjolan sistolik akhir yang terjadi ketika jantung hampir kosong
dan melakukan kontraksi yang hampir isometris. Ini merupakan temuan khas dari
kardiomiopati hipertrofik, namun lebih jarang terjadi bila dibandingkan dua
impuls apikal.
Bunyi jantung pertama normal. Bunyi jantung kedua split
secara normal, tapi pada beberapa pasien dengan gradien aliran keluar yang
parah, yang terdengar adalah paradoxical
split.
Sebuah gallop S3 umum ditemukan pada pasien
anak, tetapi tidak memiliki arti medis seburuk pada pasien stenosis katup
aorta. Ketika ditemukan pada pasien dewasa, hal ini mempertegas adanya gagal
jantung kongestif. Sebuah bunyi jantung keempat, S4, secara berkala
dapat didengar dan adalah akibat dari sistol atrial terhadap ventrikel kiri
yang sangat menurun fungsinya.
Nadi vena jugular
mengungkapkan adanya gelombang a yang prominen yang disebabkan fungsi
ventrikel kiri yang semakin berkurang dikarenakan hipertrofi masif atau adanya
septum ventrikular.
Dua denyut arterial karotis adalah umum pada keadaan ini.
Nadi karotis tersebut menaik cepat karena peningkatan kecepatan darah yang
melalui traktus aliran keluar ventrikel kiri menuju aorta. Nadi karotis
kemudian menurun pada midsistol seiring mulai timbulnya gradien. Ini kemudian
diikuti oleh kenaikan kedua pulsasi karotis pada saat sistol akhir.
Impuls apikal prekordial terkadang bergeser ke arah
lateral dan biasanya secara abnormal menguat dan melebar.
Murmur ejeksi sistolik secara umum adalah murmur
crescendo-decrescendo ejeksi sistolik, yang paling baik didengarkan diantara
apeks dan batas kiri sternal dan menjalar
ke suprasternal tetapi tidak menuju arteri karotis ataupun leher. Murmur
dan gradien yang melintasi traktus
aliran keluar ventrikel kiri, akan menurun dan berkurang seiring peningkatan
dalam preload (misalnya Mueller
maneuver, berjongkok) atau peningkatan dalam afterload (misalnya genggaman tangan). Murmur dan gradien tersebut
akan meningkat apabila ada penurunan dalam preload
(misalnya Valsalva maneuver, pemberian nitrate, pemberian diuretik, posisi
berdiri) atau dengan penurunan dalam afterload (misalnya pemberian
vasodilator).
Murmur holosistolik pada apeks dan axilla dari
regurgitasi mitral dapat didengar pada pasien dengan systolic anterior motion (SAM) yang terjadi pada katup mitral dan
gradien aliran keluar ventrikel kiri yang signifikan. Murmur decrescendo diastolik
dari regurgitasi aorta dapat didengar pada 10% pasien, walaupin regurgitasi
katup aorta ringan dapat dideteksi oleh ekokardiografi doppler pada 33% pasien.
Diagnosis
Diagnosis kardiomiopati hipertrofik didasarkan pada
sejumlah temuan pada proses terjadinya penyakit ini. Selain penggunaan
ekokardiografi, kateterisasi jantung, atau MRI jantung untuk mendiagnosis
penyakit ini, ada faktor penting lain seperti EKG dan temuan pemeriksaan
genetis (walaupun tidak digunakan sebagai pemeriksaan diagnosis utama) dan jika
terdapat riwayat anggota keluarga dengan HCM atau kematian mendadak yang tidak
dapat dijelaskan pada individu yang sebelumnya terlihat sehat.
Pemeriksaan fisik
Cara membedakan kardiomiopati hipertrofik dan stenosis katup aorta
Membedakan kardiomiopati hipertrofik dan
stenosis katup aorta
|
||
Stenosis Aorta
|
Kardiomiopati Hipertrofik
|
|
Ekokardiografi
|
||
Kalsifikasi katup aorta
|
Biasa terjadi
|
Tidak terjadi
|
Aorta ascending berdilatasi
|
Biasa terjadi
|
Jarang terjadi
|
Hipertrofi ventrikular
|
Hipertrofi ventrikel kiri konsentris
|
Asimetris, sering melibatkan septum
|
Pemeriksaan fisik
|
||
Murmur dari insufisiensi Aorta
|
Biasa terjadi
|
Tidak terjadi
|
Tekanan nadi setelah Kontaksi ventrikular prematur (PVC)
|
Meningkat
|
Menurun
|
Valsalva maneuver
|
Penurunan intensitas murmur
|
Peningkatan intensitas murmur
|
Pulsasi karotis
|
Normal atau tardus et parvus
|
Cepat tajam, menyentak atau nadi bisferiens
(kolaps denyut yang diikuti kenaikan kedua)
|
Temuan fisik dari HCM
dikaitkan dengan obstruksi aliran keluar dinamis yang sering terjadi pada
penyakit ini.
Pada saat auskultasi,
murmur jantung akan terdengar mirip dengan murmur pada stenosis aorta. Namun, murmur karena HCM meningkat
intensitasnya dengan manuver yang mengurangi volume darah pada ventrikel kiri
(seperti berdiri tiba-tiba atau saat menekan pada manuver valsava). Pemberian
amyl nitrate juga akan menegaskan murmur dengan cara pengurangan venous return ke jantung. Berdasarkan
pengalaman, murmur terdengar paling jelas pada tepi parasternal, ruang
interkosta keempat, daripada area aortik.
Jika terdapat obstruksi aliran keluar dinamis ventrikel
kiri, pemeriksaan fisik yang dapat ditemukan antara lain pulsus bisferiens dan impuls apikal ganda pada setiap kontraksi
ventrikular. Temuan ini, jika terjadi, dapat membantu membedakan HCM dengan
stenosis aorta. Sebagai tambahan, jika pasien memiliki premature ventricular contractions (PVC), perubahan pada intensitas
nadi karotis pada detak setelah PVC dapat membantu membedakan HCM dengan
stenosis aorta. Pada individu dengan HCM, tekanan nadi akan menurun pada detak
setelah PVC, sementara pada stenosis aorta, tekanan nadi meningkat. Namun,
intensitas murmur meningkat baik pada stenosis aorta maupun HCM pasca PVC.
Pertimbangan pendekatan diagnosis HCM
Ekokardiografi dua dimensi (2-D) sangat membantu dalam
diagnosis kardiomiopati hipertrofik. Secara umum, ringkasan temuan
ekokardiografi antara lain gerakan daun katup sistolik yang abnormal pada katup
mitral, hipertrofi ventrikel kiri, pembesaran atrium kiri, ukuran bilik
ventrikel yang kecil, hipertrofi septum dengan rasio septum terhadap dinding
bebas lebih besar dari 1.4:1 , prolaps katup mitral dan regurgitasi mitral,
penurunan aliran midaortik, dan penutupan sistolik sebagian dari katup aorta
pada midsistol.
Magnetic resonance imaging (MRI) jantung juga membantu
dalam diagnosis dan assessment HCM. Tidak
ada pemeriksaan darah laboratoris spesifik yang diperlukan dalam
penatalaksanaan HCM. Pemeriksaan genetik tidak tersedia secara luas untuk saat
ini tetapi menjadi semakin banyak seiring dengan waktu untuk kondisi penyakit
ini. Dalam situasi penelitian atau
dengan riwayat keluarga yang luas, genotyping menjadi informatif untuk
identifikasi anggota keluarga tambahan jika genotype penderita utama telah
ditentukan.
Ekokardiografi dua dimensi dan penelitian Doppler
Sebagaimana disebutkan di atas, ekokardiografi
dua dimensi bersifat diagnostik untuk kardiomiopati hipertrofik. Studi aliran Doppler berwarna umumnya mampu mengungkapkan regurgitasi
mitral. (gambar bawah)
Studi Doppler continuous-wave
pada HCM obstruktif mengungkap adanya peningkatan kecepatan aliran yang
melintasi traktus aliran keluar ventrikel kiri. HCM obstruktif parah biasanya
memiliki kecepatan aliran lebih besar dari 4 m/s, dan gradien yang melintasi
traktus aliran keluar ventrikel kiri lebih besar dari 50 mm Hg sudah dianggap parah.
Ekokardiografi juga biasanya mengungkap adanya disfungsi
diastolik dengan fungsi ventrikel kiri yang berkurang dan rasio katup mitral
dari gelombang E terhadap gelomban A lebih kecil dari 1 (biasanya < 0.8).
Fungsi sistolik umumnya terjaga baik dan normal, bahkan fraksi ejeksi ventrikel
kiri biasanya normal atau lebih tinggi pada saat diagnosis. Diameter ventrikel
kiri ada pada batas bawah normal atau lebih kecil dari normal.
Sebuah studi yang dilakukan oleh Peteiro et al mengemukakan
bahwa assessment terhadap kapasitas aktivitas fisik dan fungsi sistolik
ventrikel kiri selama ekokardiografi latihan fisik dapat membantu dalam
menentukan tingkatan risiko diantara pasien dengan kardiomiopati hipertrofik.
Imaging /
Pencitraan jaringan dengan Doppler cukup bermanfaat sebagai sarana screening pada pasien dengan ventrikel
yang secara morfologis normal dan dalam membedakan HCM dengan penyebab lain
hipertrofi ventrikel kiri (misal hipertrofi jantung atlet).
Tanda khas dari HCM tipe obstruktif terdiri dari adanya gerakan anterior sistolik
/ systolic anterior motion (SAM) dari daun katup anterior katup mitral,
ketebalan dinding septum > 15 mm, dan
hipertrofi septum asimetris dengan rasio ketebalan dinding septum terhadap
ketebalan dinding posterior lebih besar dari 1.4:1.
Septum bukan hanya relatif lebih tebal dari dinding
posterior, tetapi biasanya 4-6 mm lebih tebal dari normal pada setiap kelompok
umur. Hipertrofi masif dengan ketebalan dinding septum lebih besar dari 25 mm pernah
tercatat dalam kasus langka, khususnya pada bayi dengan defek penyimpanan
glikogen, sebagaimana diobservasi pada pasien dengan penyakit Pompe.
Sebuah pola ekokardiografik tidak wajar yang terdiri dari
penampakan ground-glass pernah
tercatat pada beberapa bagian miokardium yang mengalami hipertrofi pada
beberapa pasien. Pola ini mungkin berkaitan dengan struktur arsitektur cellular
abnormal dan fibrosis miokardial yang telah diamati pada beberapa studi
patologis
Penyempitan traktus aliran keluar ventrikel kiri terjadi
pada banyak pasien dengan HCM. Hal ini berkontribusi terhadap terjadinya
gradien tekanan pada sejumlah kecil pasien. Tanda khas HCM yang berkaitan
dengan tekanan gradien adalah SAM (gerakan sistolik anterior) yang abnormal
dari katup mitral, dan pada kasus yang jarang, gerakan sistolik dari daun katup
posterior.
Banyak temuan ekokardiografis lainnya dapat ditemukan
pada pasien dengan HCM. Sebagai contoh, kavitas ventrikel kiri yang kecil dapat
ditemukan sebagai akibat dari hipertrofi miokardium yang jelas dan kelainan
pada kavitas ventrikel kiri. Terlebih
lagi, pengurangan pergerakan dan penebalan septum selama sitol dapat terjadi,
khususnya pada septum bagian atas, yang merupakan akibat dari ketidakteraturan
arsitektur miofibril dan fungsi kontraktilitas yang abnormal.
Pergerakan dinding posterior dapat normal atau meningkat,
dan kecepatan penutupan katup mitral pada middiastol dapat berkurang yang
diakibatkan penurunan fungsi ventrikel kiri atau aliran lintas mitral yang
abnormal pada saat diastol. Sebagai tambahan, prolaps katup mitral, sebuah
kejadian ekokardiografik HCM yang jarang, dapat ditemukan..
Penutupan sistolik parsial, atau yang lebih umum, gerakan
mengepakkan yang kasar dari katup aorta yang berkaitan dengan turbulensi aliran
darah pada traktus aliran keluar dapat terjadi. Kelainan dalam fungsi diastolik
dapat ditunjukkan oleh perekaman ekokardiografi dan Doppler pada sekitar 80%
pasien dengan HCM, dengan atau tanpa adanya gradien tekanan sistolik.
Adanya regurgitasi mitral hampir selalu dapat dikonfirmasi
oleh ekokardiografi Doppler pada pasien HCM dengan gradien sistolik.
Dasar
diagnosis dari kardiomiopati hipertrofik adalah dengan menggunakan
ekokardiogram karena dapat menggambarkan ketebalan ukuran ventrikel dan fungsi
sistolik, yang memperlihatkan hipertropi ventrikel kiri yang asimetris terutama
mengenai septum interventrikel.
Dengan ekokardiografi
dapat dibedakan beberapa jenis hipertrofi ventrikel kiri yaitu asimetrik septal
hipertrofi (septum ventrikel 90%, mid ventrikel 1%, apeks 1%, posteroseptal dan
dinding lateral 1%) dan simetrik hipertropi (5%). Pada ekokardiografi
ditemukan pengecilan rongga ventrikel kiri, penebalan septum ventrikel
dibandingkan dengan dinding posterior ventrikel kiri dengan rasio>1,5:1,
penurunan derajat penutupan katup mitral, systolic
anterior motion (SAM) katup
mitral, obstruksi jalur keluar ventrikel kiri, imobilitas relatif septum
ventrikel dengan kontraksi yang hebat dinding posterior.
Bentuk yang jarang dari kardiomiopati hipertrofik,
mempunyai karakteristik hipertrofi apikal, yang biasanya berhubungan dengan
gelombang negatif T raksasa pada elektrokardiogram (EKG) dan mempunyai gambaran
cavitas ventrikel kiri yang berbentuk “spade
shaped” pada angiography; dan biasanya mempunyai onset klinis yang jinak.
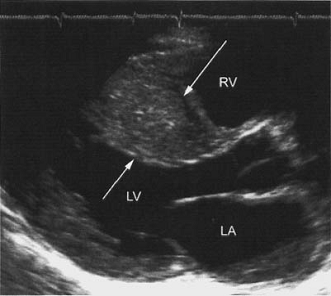 |
| Gambar Asymmetric septal hypertrophy |
Pada gambar di atas
tampak gambaran penonjolan septum yang hipertrofi yang tampak jelas pada daerah
parasternal (yang ditunjuk anak panah).
 |
| Gambar Kardiomiopati hipertrofi apikal |
Pencitraan (Imaging) Radiografi
dan Radionuklir dada
Radiografi dada
Temuan radiografi dada / Chest radiograph (CXR) dapat beragam. Silhouette jantung dapat beragam dari normal sampai dengan
peningkatan ukuran yang signifikan. Pembesaran atrium kiri sering teramati,
khususnya jika terdapat regurgitasi mitral yang signifikan. Hal ini
bermanifestasi dengan penampakan "double-density" pada CXR.
Pencitraan Radionuklir
Pencitraan radionuklir dengan thallium atau technetium dapat
menunjukkan defek yang reversibel, terutama jika tidak ditemukan penyakit
arteri koroner. Scintigraphy (skintigrafi) thallium atau technetium dapat mengungkap kelainan
pada perfusi miokardial, bahkan pada kondisi arteri koroner yang tampak normal
secara angiografis..
Defek reversibel yang dibuktikan oleh scanning radionuklir ini lebih umum
ditemukan pada anak atau remaja dengan riwayat sinkop dan kematian jantung
mendadak, sehingga diperkirakan iskemia miokard merupakan faktor penting dalam
mekanisme fatalitas pada pasien muda dengan HCM.
MRI jantung
Pencitraan MRI jantung sangat berguna dalam diagnosis dan
assessment HCM, dengan kualitas citra yang ideal dapat mencakup keseluruhan dua
ventrikel untuk mengetahui lokasi tepat hipertrofi. MRI jantung secara khusus
bermanfaat ketika hasil ekokardiografi dipertanyakan, misalnya dengan
hipertrofi apikal.
Pencitraan cine
(dinamis) MRI, yang berorientasi pada area traktus aliran keluar ventrikel
kiri, biasanya menunjukkan obstruksi, dan pemetaan kecepatan berguna dalam
assessment kecepatan (velocity)
puncak. SAM (Systolic anterior motion)
dari katup mitral dapat dengan jelas terlihat pada MRI jantung.
Perkembangan obstruksi setelah ablasi septum atau
miomektomi dapat ditunjukkan, begitu juga lokasi dan ukuran infark yang
berkaitan, sehingga berguna dalam perencanaan tindakan medis berikutnya.
Penandaan (tagging)
MRI jantung dapat mengidentifikasi pola abnormal dari peregangan, kerusakan dan
torsi dari kasus HCM, yang menunjukkan disfungsi signifikan pada area
hipertrofik dari ventrikel. Cardiovascular
MR spectroscopy (spektroskopi resonansi magnetis kardiovaskular) dapat
mengungkap kelainan bioenergetik pada pasien HCM dengan mutasi genetik yang
beragam, fakta yang dapat mendukung hipotesis bahwa unsur yang mendasari
terjadinya HCM adalah penggunaan (utilisasi) energi yang tidak efisien.
Akurasi penentuan fenotipik HCM oleh MRI jantung berguna
pada screening anggota keluarga, dan
studi keterkaitan genetik untuk mutasi penyebab menjadi lebih terbantu.
Penggunaan kontras gadolinium pada MRI jantung sangat
bermanfaat dalam membedakan HCM dengan penyebab hipertrofi jantung lainnya dan
jenis kardiomiopati lain, seperti amiloidosis, jantung atlet, penyakit Fabry
(defisiensi alpha-galactoside).
Gadolinium yang terlihat jelas pada saat akhir pada HCM
menunjukkan adanya fibrosis miokardial. Semakin besar derajat kejelasan
penampakan gadolinium yang terjadi saat akhir,
semakin mungkin pasien HCM tersebut memiliki 2 atau lebih faktor untuk
kematian mendadak dan lebih mungkin terjadinya perkembangan pelebaran
(dilatasi) ventrikular yang mengarah kegagalan jantung, sehingga
mengindikasikan prognosis yang lebih buruk.
Kebanyakan pasien dengan HCM tidak memiliki kejelasan
penampakan gadolinium , pola jinak yang
umum ditemukan adalah 2 garis yang berjalan sepanjang persimpangan ventrikel
kanan yang memasuki ventrikel kiri.
Penampakan kejelasan gadolinium dapat berupa penampakan
padat, seperti plak, atau difus (menyebar). Semakin jelas penampakan gadolinium, semakin
tinggi kegagalan jantung atau kematian mendadak, diduga dari takikardia reentrant atau kegagalan sistolik karena
pergeseran miosit.
Penyakit Fabry (defisiensi
alpha-galactoside), yang terjadi pada sekitar 4% pasien HCM, sering menunjukkan
penampakan gadolinum tidak wajar pada dinding lateral dengan MRI jantung.
 |
| Gambar di atas merupakan gambar kardiomiopati hipertrofi simetrik yang memperlihatkan hipertrofi difus dari dinding ventrikel kiri dan kanan. |
Elektrokardiogram (ECG)
Temuan elektrokardiografi yang umum ditemukan diantaranya
abnormalitas gelombang ST-T dan hipertrofi ventrikel kiri. Temuan
lain yang teramati pada EKG adalah deviasi axis (kanan atau kiri), abnormalitas
konduksi (P-R memanjang, bundle-branch block), sinus bradikardia dengan irama
atrial ektopik, dan pembesaran atrial. Satu
mutasi telah mengaitkan antara kardiomiopati hipertrofik dan sindrom
Wolff-Parkinson-White.
Temuan tidak umum diantaranya gelombang Q yang abnormal
dan menonjol pada lead anterior prekordial dan tungkai lateral, interval P-R
pendek dengan QRS yang diduga adalah preeksitasi, fibrilasi atrial (tanda
prognostik buruk), dan abnormalitas gelombang P, menandakan diantaranya
pembesaran atrium kiri.
Temuan pada pengawasan Holter dan elektrokardiografi kejadian biasanya terdiri dari ektopi
atrial dan ventrikular, jeda sinus, wandering atrial pacemaker, takikardia
atrail, fibrilasi atrial dan/atau flutter, takikardia ventrikular nonsustained.
Pemeriksaan kardiovaskular komprehensif dengan MRI dapat
menemukan bekas perlukaan dan mungkin dapat membantu memprediksi segala
penyebab dan kematian jantung pada pasien HCM dengan sedikit gejala atau
asimtomatik.
 |
| Gambaran EKG pasien dengan apikal hipertropi dengan prekordial inversi gelombang T |
Kateterisasi Jantung
Pada kateterisasi jantung, kateter dapat dipasang pada
ventrikel kiri dan aorta ascending, untuk mengukur perbedaan tekanan pada kedua
struktur ini. Pada individu normal selama sistol ventrikular, tekanan pada
aorta ascending dan ventrikel kiri akan sama, dan katup aorta akan terbuka.
Pada individu dengan stenosis aorta atau dengan HCM dengan gradien traktus aliran keluar
(outflow), akan terjadi gradien (perbedaan) tekanan antara ventrikel kiri dan
aorta tersebut, dengan tekanan pada ventrikel kiri lebih besar daripada tekanan
aorta. Gradien ini merupakan representasi derajat obstruksi yang harus
terlewati dalam rangka memompa darah dari ventrikel kiri.
Tanda Brockenbrough–Braunwald–Morrow
teramati pada pasien dengan HCM yang memiliki gradien outflow tract (traktus/jalur aliran keluar). Tanda ini dapat
digunakan untuk membedakan HCM dengan stenosis aorta. Pada individu dengan
stenosis aorta, setelah terjadinya premature
ventricular contraction (PVC), kontraksi ventrikular berikutnya akan lebih
kuat dan tekanan yang dihasilkan pada
ventrikel kiri akan lebih tinggi. Dikarenakan obstruksi yang terfiksasi pada
stenosis katup aorta, tekanan aorta pasca PVC akan ikut serta meningkat. Namun
pada individu dengan HCM derajat obstruksi akan meningkat lebih dari peningkatan
kekuatan kontraksi yang terjadi pasca detak PVC. Hal ini akan mengakibatkan
peningkatan tekanan pada ventrikel kiri dan tekanan pada aorta ascending
menurun, diiringi peningkatan gradien LVOT (left
ventricular outflow tract/ traktus aliran keluar ventrikel kiri).
Walaupun tanda Brockenbrough–Braunwald–Morrow
dapat terlihat paling baik dengan kateter intra-kardiak dan intra-aorta yang
berlangsung bersamaan, tanda ini juga dapat ditemukan pada pemeriksaan fisik
rutin dengan penurunan tekanan nadi pada detak pasca PVC pada individu dengan
HCM.
Walaupun tidak dibutuhkan untuk diagnosis kardiomiopati
hipertrofik, sebuah kateterisasi jantung diagnostik bermanfaat untuk menentukan
derajat obstruksi aliran keluar, hemodinamik jantung, karakteristik diastolik
ventrikel kiri dan anatomi ventrikel kiri, dan yang cukup penting, anatomi
koroner. Kateterisasi jantung juga dilaksanakan pada situasi ketika terapi
dengan metode invasif, seperti pemasangan pacemaker atau pembedahan, sedang
direncanakan.
Intervensi terapi dengan kateterisasi jantung, dilaksanakan
pada kasus kardiomiopati hipertrofik yang khusus dan terpilih, diantaranya
adalah ablasi alkohol transkateter septal untuk mengurangi obstruksi aliran
keluar ventrikel kiri dengan infark yang disengaja pada sebagian septum
interventrikular.
Kateterisasi jantung terkadang mengurangi fungsi
diastolik ventrikel kiri dan, pada kasus hipertrofik kardiomiopati obstruktif, menimbulkan
sebuah tekanan gradien sistolik intrakavitas di dalam ventrikel kiri yang
berkaitan dengan SAM subaorta katup mitral yang berbatasan dengan septum yang
mengalami hipertrofi. Tekanan gradien subaorta tersebut dapat menjadi cukup
labil dan dapat bervariasi antara 0 dan 175 mmHg pada pasien yang sama dengan
kondisi yang berbeda.
Pelacakan pembacaan hasil tekanan arterial yang ditemukan
pada kateterisasi jantung dapat
menunjukkan konfigurasi “kerucut dan kubah” mirip dengan perekaman nadi
karotis. Sebagai konsekuensi fungsi ventrikel kiri yang berkurang; mean arterial pressure (MAP) kiri dan,
khususnya gelombang a, pada
tekanan nadi atrial kiri dan tekanan end-diastolic ventrikel kiri biasanya
mengalami peningkatan.
Artefak gradien aliran keluar dapat terjadi jika kateter
ventrikel kiri terperangkap dalam trabekula dari sebuah hipertrofi ventrikel
kiri. Cardiac output dapat terdepresi
pada pasien dengan gradien parah yang berlangsung lama, tetapi pada mayoritas
pasien tidak terjadi. Terkadang, cardiac
output meningkat pada pasien dengan fungsi sistolik ventrikel kiri yang
hiperdinamis secara signifikan.
Abnormalitas hemodinamik pada HCM tidak terbatas pada
sisi kiri dari jantung. Sekitar satu dari empat pasien menunjukkan hipertensi
pulmonal. Biasanya ringan, namun pada beberapa kasus, dapat menjadi sedang
sampai dengan berat/parah, dikarenakan (setidaknya sebagian) oleh peningkatan
mean atrial pressure (MAP) kiri yang diakibatkan fungsi ventrikel kiri yang
menurun. Sebuah gradien tekanan pada traktus aliran keluar ventrikel kanan terjadi pada sekitar 15%
pasien yang memiliki obstruksi aliran keluar ventrikel kiri dan tampaknya
merupakan hasil dari hipertrofi signifikan dari janringan ventrikel kanan.
Tekanan end-diastolic ventrikel kanan dan atrial kanan dapat sedikit mengalami
kenaikan.
Keberagaman Outflow gradient
Salah satu fitur karakteristik HCM adalah outflow gradient (gradien aliran keluar)
ventrikl kiri yang beragam dan labil. Seorang pasien dapat menunjukkan gradien
yang besar pada satu masa dan tidak menunjukkan sama sekali pada waktu yang
lain. Pada beberapa pasien tanpa adanya gradien waktu beristirahat, terkadang
dapat terprovokasi dan timbul sementara.
Tiga mekanisme dasar yang terlibat dalam
terjadinya gradien dinamis adalah peningkatan kontraktilitas, penurunan
preload, dan penurunan afterload. Pada banyak pasien dengan HCM, gradien
terletak midventrikular dan dapat diintensifkan dengan peningkatan kontraktilitas,
yang mengakibatkan gerakan sfincter muskulus langsung.
Rangsangan yang memprovokasi atau mengintensifikasi
gradien LVOT pada HCM secara umum memperbaiki kinerja miokardial pada individu
normal atau pasien dengan kelainan jantung tertentu lainnya. Pengurangan
kontraktilitas atau peningkatan preload atau afterload, akhirnya akan
meningkatkan dimensi ventrikel kiri dan
mengurangi atau menghilangkan gradien LVOT..
Salah satu rangsangan ampuh untuk meningkatkan gradien
LVOT adalah potensiasi pasca ekstrasistolik, yang dapat terjadi setelah
kontraksi prematur spontan atau ditimbulkan stimulasi mekanis dengan kateter.
Resultan peningkatan kontraktilitas pada detak setelah ekstrasistol begitu
signifikan sehingga menghasilkan peningkatan pada gradien outflow. Sebuah perubahan khas sering terjadi pada perekaman
perjalanan tekanan arteri yang dilakukan secara langsung, yang selain
menampakkan konfigurasi kerucut dan kubah yang menonjol, juga menunjukkan
tekanan nadi yang gagal meningkat sesuai seharusnya atau bahkan menurun
(dinamakan fenomena Brockenbrough-Braunwald).
Ini merupakan salah satu tanda yang dapat diandalkan akan
adanya obstruksi dinamis pada LVOT. Pada beberapa pasien, murmur pasca
ekstrasistolik melemah meskipun terjadi peningkatan pada gradien outflow,
tampaknya dikarenakan, pada situasi ini, murmur lebih mengikuti perubahan yang
lebih besar pada keparahan regurgitasi mitral ketimbang perubahan pada
LVOT.
Ventrikulografi Kiri
Ventrikulografi kiri secara khas dapat menunjukkan
ventrikel hipertrofi dan adanya gradien outflow. Daun katup anterior dari katup
mitral begerak secara anterior selama sistol dan mengikuti jalur aliran keluar
(outflow tract). Yang diasosiasikan
dengan gerakan ini adalah regurgitasi mitral, yang merupakan temuan sering pada
pasien dengan gradien. Kavitas ventrikel kiri seringkali kecil, dengan ejeksi
sitolik yang biasanya kuat, maka pada akhir sistol ventrikel kiri akan seperti
menghilang dikarenakan ukurannya yang semakin kecil. Pada pasien dengan
keterlibatan apikal, hipertrofi yang ekstensif dapat membentuk suatu
konfigurasi menyerupai sekop (spade-like) pada angiogram ventrikular kiri.
Temuan lain
Pada pasien berusia lebih dari 45 tahun, penyakit arteri
koroner obstruktif kemungkinan dapat ditemukan, walaupun gejala dari nyeri
iskemik sulit dibedakan dengan gejala yang sama dari pasien dengan angiogram
koroner normal dan HCM. Arteri descending sinistra dan arteri koroner
perforator septal dapat menunjukkan penyempitan bertahap dan abnormalitas
terkait aliran selama sistol.
Studi Elektrofisiologik
Sebuah studi elektrofisiologi diagnostik yang menggunakan
stimulasi listrik yang terprogram dapat mengidentifikasi kelainan konduksi,
disfungsi sinus node / sinus node
dysfunction (SND), dan potensi akan aritmia yang diinduksi.
Korelasi prognostik pada
aritmia yang diinduksi dengan aritmia
klinis spontan dan/atau kematian mendadak belum jelas secara keseluruhan.
Beberapa studi menunjukkan hubungan antara hasil elektrofisiologik dan pemeringkatan
risiko akan kematian mendadak, tapi studi lain tidak dapat menunjukkan hubungan
langsung.
Temuan histologis
Hipertrofi miokardial dan ketidakteraturan jaringan otot
yang mengakibatkan suatu pola khas berbentuk spiral, kekacauan susunan sel dan
disorganisasi struktur miofibril di dalam sel, terjadi pada hampir semua pasien
dengan kardiomiopati hipertrofik.
Fibrosis cukup menonjol ditemukan dan mungkin menjadi
cukup ekstensif untuk menghasilkan
penampakan bekas perlukaan yang besar. Intramural arteri koroner abnormal,
dengan pengurangan ukuran lumen dan penebalan dinding pembuluh, adalah temuan
umum pada pasien dengan HCM, terjadi pada lebih dari 80% kasus. Kelainan ini
lebih sering terjadi pada septum ventrikular dan mendampingi fibrosis ekstensif
pada dinding jantung yang terpengaruh.
Pertimbangan pendekatan
Prinsip dasar terapi pengobatan dan pembedahan adalah
digunakan untuk mengurangi kontraktilitas ventrikular atau meningkatkan volume
ventrikular, meningkatkan fungsi (compliance) ventrikular dan dimensi traktus
aliran keluar (outflow tract), dan pada kasus HCM obstruktif, mengurangi
gradien tekanan sepanjang LVOT. Yang terpenting dari semua terapi adalah
pengurangan risiko kematian mendadak dengan mengidentifikasi pasien ini pada
tahap awal dan pengobatan yang efektif dan/atau implantasi pembedahan defibrilattor
otomatis.
Pengobatan diantaranya adalah beta blocker, calcium
channel blocker, dan walaupun jarang : diltiazem, amiodarone, dan disopyramide.
Antitusif dapat diberikan untuk menghindari batuk.
Penelitian menunjukkan bahwa terapi bertahap dapat mengurangi
tekanan darah tinggi pada pasien dengan HCM. Pada studi dengan 115 pasien HCM,
termasuk didalamnya 94 pasien dengan HCM obstruktif, terapi hipertensi bertahap
secara efektif mengendalikan baik gejala HCM obstruktif maupun hipertensi.
Tekanan sistolik rata-rata pada kelompok HCM obstruktif berkurang dari 137 ke
131 mm Hg, dan hipertensi tidak terkendali berkurang dari 56% pada kunjungan
pertama menjadi 37% pada kunjungan terakhir.
Hindari obat inotropik jika dimungkinkan; Juga hindari
nitrat dan amina simpatomimetik, kecuali pada pasien yang juga mengalami
penyakit arteri koroner. Hindari digitalis, karena glikosida adalah
kontraindikasi kecuali pada pasien dengan fibrilasi atrial tidak terkendali.
Kewaspadaan terhadap penggunaan diuretik perlu diterapkan karena potensi efek
merugikan terhadap gradien LVOT dan volume ventrikular.
Pencegahan
Pasien harus menghentikan untuk melakukan aktivitas
atletis kompetitif yang berkelanjutan dan kegiatan fisik berat yang menggunakan
banyak tenaga, seperti mencangkul atau mengangkat beban berat, dikarenakan
risiko kematian jantung mendadak aritmogenik. Rekomendasi pengobatan dan pencapaian
penyembuhan tidak pernah menyimpang dari larangan aktivitas-aktivitas tersebut.
Konsultasi
Untuk penatalaksanaan
dan pemahaman komprehensif penyakit ini, konsultasi dapat dilakukan dengan dan
antara :
- Kardiologis
- Spesialis bedah toraks dan
kardiovaskular
- Ahli elektrofisiologi
- Ahli genetika
Diet
Tidak ada diet (batasan
makanan) khusus. Namun pasien seharusnya menghindari kenaikan berat badan yang
eksesif.
Obat-obatan (Medikamentosa)
Tujuan utama dari pemberian obat-obatan adalah mengurangi gejala seperti nyeri dada, sesak nafas, dan palpitasi. Beta blocker dianggap sebagai agen lini pertama, karena mereka dapat memperlambat heart rate dan mengurangi kemungkinan terjadinya detak ektopik. Pada pasien yang tidak dapat mentoleransi beta blocker atau tidak mengalami perbaikan gejala dengan beta blocker, calcium channel blocker nondihidropiridin seperti verapamil dapat digunakan, walaupun berpotensi berbahaya pada pasien dengan keadaan hipotensi sistemik atau dyspnea parah pada saat istirahat. Obat ini juga menurunkan heart rate, walau pengunaannya pada pasien dengan obstruksi outflow parah, peningkatan tekanan oklusi arteri pulmonal dan tekanan darah rendah, harus dilakukan dengan kewaspadaan. Dihydropyridine calcium channel blockers seharusnya dihindari pada pasien dengan bukti adanya obstruksi. Pada pasien yang tetap memiliki gejala walaupun sudah diberikan penanganan di atas, disopyramide dapat dipertimbangkan untuk perbaikan atau pengurangan gejala. Diuretik dapat diberikan pada pasien dengan bukti adanya overload cairan, walaupun harus digunakana dengan kewaspadaan dengan bukti adanya obstruksi. Pasien yang tetap memiliki gejala walaupun diberikan terapi obat dapat mempertimbangkan terapi yang lebih invasif. Phenylephrine intravena (atau agen vasokonstriksi murni lainnya) dapat digunakan pada situasi hipotensi akut dengan kardiomiopati hipertrofik yang tidak memberikan respons terhadap pemberian cairan.
Miomektomi Ventrikel Kiri dan Perbaikan Katup Mitral
Miomektomi Ventrikel Kiri
Miomektomi ventrikel kiri dilaksanakan pada pasien gejala
parah dan tidak membaik dengan terapi serta memiliki gradien outflow lebih dari
50 mm Hg, baik pada saat istirahat maupun dengan aktivitas yang memprovokasi.
Prosedur miomektomi ini umumnya sukses dalam menghilangkan gradien outflow;
kebanyakan pasien mendapatkan perbaikan gejala pada paling tidak 5 tahun
berikutnya.
Pengurangan gradien LVOT mungkin tidak akan berkorelasi
dengan pengurangan risiko kematian mendadak atau mortalitas secara keseluruhan.
Ditambah lagi, gradien outflow dapat meningkat secara bertahap seiring dengan
waktu dan kembali seperti keadaan sebelumnya, sehingga mengakibatkan perlunya
pengulangan prosedur atau terapi pengobatan tambahan. Pasien dengan HCM
obstruktif dengan gradien istirahat yang rendah dan obstruksi laten mungkin
dapat memiliki gejala merugikan yang sama dengan pasien yang memiliki gradien
istirahat yang parah. Pada 749 pasien yang menjalani miektomi septal, 249 memiliki
gradien pada saat istirahat yang rendah tetapi memiliki obstruksi traktus
outflow yang parah dengan uji provokasi. Perbaikan gejala dan ketahanan hidup pada pasien-pasien ini
serupa dengan pasien dengan obstruksi outflow parah pada saat istirahat yang
menjalani miektomi. Sehingga dapat disarankan miektomi septal direkomendasikan
pada pasien yang memiliki obstruksi outflow parah hanya pada uji provokasi
karena ketahanan hidup dan perbaikan gejala adalah baik, yang dapat diartikan
obstruksi dinamis adalah masalah hemodinamik yang utama, bukan disfungsi
diastolik.
Pembedahan septal miektomi adalah operasi jantung terbuka
yang dilakukan untuk perbaikan gejala pada pasien yang tetap simtomatik berat
meskipun sudah dilakukan terapi pengobatan. Tindakan ini telah sukses dilakukan
selama lebih dari 25 tahun. Pembedahan miektomi septal prinsipnya mengurangi
obstruksi LVOT dan memperbaiki gejala, dan pada pusat pelayanan kesehatan yang
berpengalamanan memiliki angka mortalitas pembedahan kurang dari 1% dan juga
angka sukses 85%. Tindakan ini terdiri
dari sternotomi median (anestesi umum, pembukaan dada, dan bypass
kardiopulmonal) dan mengambil dan membuang sebagian dari septum
interventrikular. Reseksi miektomi yang hanya berfokus pada septum subaortik,
untuk memperbesar ukuran outflow tract
agar mengurangi gaya Venturi mungkin tidak cukup untuk menghilangkan total
gerakan sistolik anterior / systolic
anterior motion (SAM) dari daun katup anterior dari katup mitral. Dengan
jenis reseksi yang terbatas ini, tonjolan mid-septal yang tersisa tetap
mengarahkan aliran secara posterior. SAM tetap ada karena aliran mengalir
dibelakang katup mitral. Hanya jika bagian yang mendalam dari tonjolan septal
yang direseksi sehingga aliran dialirkan secara anterior menjauh dari katup
mitral, maka akan terjadi menghilangnya atau terhapusnya SAM. Dengan catatan
tersebut, sebuah modifikasi miektomi diperpanjang dari apa yang dikenal sebagai
miektomi Morrow, mobilisasi dan eksisi parsial dari muskulus papilaris telah
menjadi eksisi pilihan. Pada pasien tertentu dan terpilih dengan katup mitral
yang redundan (berlebihan), plication
(lipatan) daun katup anterior dapat ditambahkan untuk melengkapi pemisahan
katup mitral dan outflow. Komplikasi
dari pembedahan miektomi septal diantaranya kemungkinan kematian, aritmia,
infeksi, perdarahan terus-menerus, perforasi/defek septal, stroke.
Penggantian Katup Mitral
Penggantian katup mitral
dikhususkan untuk pasien dengan regurgitasi mitral parah yang disebabkan
gerakan sistolik anterior (SAM) dari katup mitral, khususnya ketika regurgitasi
/ insufisiensi mitral (fraksi regurgitan luas) diasosiasikan dengan perkembangan
gagal jantung kongestif atau hipertensi pulmonal parah.
Implantasi Pacemaker (alat pacu jantung)
Panduan The ACC/AHA/HRS 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities
merekomendasi pacu (pacing) permanen untuk SND (sinus node dysfunction) atau AV block pada pasien dengan HCM dan
dapat dipertimbangkan pada pasien HCM yang gejalanya tidak membaik dengan
pengobatan dan obstruksi LVOT yang signifikan baik pada saat istirahat maupun
terprovokasi.
Metode transvenous
dual-chamber pacing telah digunakan untuk pasien dengan HCM. Preeksitasi
septal ventrikel kanan disebabkan oleh pacing
apikal ventrikel kanan yang mengakibatkan “menarik dirinya” septum dari daerah outflow, sehingga terjadi peningkatan
dalam aliran dan pengurangan obstruksi LVOT.
Banyak pasien merasakan perbaikan gejala dengan
implantasi pacemaker dan dapat
mengurangi obat-obatan yang harus diminum.
Perlu dicatat pengurangan dalam gradien LVOT bukan berarti
akan terjadi pengurangan dalam kerentanan terjadinya aritmia ventrikular dan
kematian mendadak. Sehingga, pacing
permanen pada pasien dengan HCM diposisikan sebagai terapi pelengkap oleh
beberapa peneliti dibandingkan sebagai penatalaksanaan utama. Hasil yang
dilaporkan sangat beragam, dengan efek plasebo signifikan dan keberagaman hasil akhir pasien.
Penggunaan pacemaker
telah disarankan pada sejumlah individu, dalam rangka menimbulkan kontraksi
asinkron dari ventrikel kiri. Dikarenakan pacemaker mengaktivasi septum
interventrikular sebelum dinding bebas ventrikel kiri, gradien sepanjang LVOT
dapat menurun. Terapi semacam ini telah menunjukkan memberikan perbaikan gejala
yang lebih sedikit dan pengurangan gradien LVOT yang lebih sedikit jika
dibandingkan pembedahan miektomi. Kemajuan teknologi juga telah mengembangkan
pacemaker dua bilik, yang hanya menyala / bekerja pada saat dibutuhkan (berbeda
dengan pacemaker biasa yang menyediakan stimulus konstan). Walaupun pacemaker
dua bilik telah menunjukkan dapat menurunkan obstruksi LVOT, penelitian
percobaan menemukan hanya beberapa individu yang mengalami perbaikan gejala. Dan
sayangnya, peneliti menduga bahwa laporan “perbaikan” gejala ini dikarenakan
efek plasebo.
Prosedur ini diantaranya adalah insisi dari area
anterlateral dibawah klavikula. Dua lead kemudian dimasukkan, satu pada atria
kanan dan yang satu lagi kedalam apeks ventrikel kanan melalui vena subklavia.
Ketika sudah ditempatkan, lead-lead ini diamankan dan dihubungkan ke generator
yang akan tetap berada di dalam fascia pasien, yeng terletak anterior terhadap
otot pektoral. Komplikasi dari prosedur ini diantaranya infeksi, kerusakan lead
listrik dan generator sehingga akan membutuhkan penggantian.
Kateter Ablasi Septal
Ablasi septal alkohol
diperkenalkan oleh Ulrich Sigwart pada tahun 1994, adalah
suatu teknik perkutaneus yang melibatkan injeksi alkohol kedalam salah satu
atau lebih cabang septal dari arteri descending sinsitra anterior. Ini
merupakan teknik yang hasilnya mirip dengan prosedur pembedahan miektomi septal
tetapi lebih tidak invasif, karena tidak memerlukan anestesia umum dan
pembukaan dinding dada dan perikardium (yang dilakukan pada miektomi
septal). Pada populasi tertentu dengan
gejala yang jelas disebabkan oleh gradien outflow
tract yang tinggi, ablasi septal ini dapat mengurangi gejala dari HCM.
Sebagai tambahan, individu yang berusia tua dan mereka yang memiliki masalah
kesehatan lainnya, yang akan meningkatkan risiko prosedural pada pembedahan
miektomi, akan mendapatkan manfaat dari prosedur ablasi septal yang lebih tidak
invasif.
Ketika dilaksanakan secara tepat, ablasi septal alkohol
akan menimbulkan suatu serangan jantung yang terkendali, dimana suatu bagian
dari septum interventrikular yang melibatkan LVOT menjadi infark dan akan
berubah menjadi bekas perlukaan (scar).
Pasien mana yang paling tepat diberikan pembedahan miektomi, ablasi septal
alkohol, atau terapi obat adalah topik yang penting dan diperdebatkan secara
intens pada kalangan ilmuwan medis.
Prosedur ablasi kateter transvena dari area septal telah
dilaksanakan menggunakan infusi etanol arterial selektif untuk menghancurkan
jaringan miokardial. Prosedur ini melibatkan infus 96% ethanol kedalam cabang
septal pertama dari arteri descending anterior sinistra dan menimbulkan suatu
infark terapi pada miokardium proksimal septal interventrikular.
Hal ini akan mengakibatkan perubahan bentuk (remodelling)
septum, yang akan mengurangi ketebalan yang signifikan dari septum, yang
merupakan ciri khas HCM, serta mengakibatkan pengurangan gradien sepanjang LVOT.
Karena kondisi ini, prosedur ini disamakan dengan pembedahan miomektomi, dalam
upayanya untuk mengurangi jumlah miokardium septal ventrikular sehingga terjadi
penurunan gradien LVOT.
Prosedur ini telah dilakukan secara klinis sejak tahun
1990an dan hasil yang dilaporkan sangat baik, dengan pengurangan signifikan
dalam gejala, dan insidensi kegagalan jantung. Pada banyak pusat pelayanan
kesehatan, ini merupakan prosedur pembedahan pilihan untuk HCM.
Implantable Cardioverter Defibrillator
Implantable cardioverter
defibrillator (ICD) telah digunakan sebagai pencegahan
kematian mendadak yang dikarenakan aritmia. Penempatan transvena mirip dengan
teknik pada implantasi pacemaker permanen dan dapat dilakukan di ruangan
laboratorium elektrofisiologi maupun pembedahan.
Sebuah ICD akan
secara otomatis mendeteksi, mengenali, dan menangani takiaritmia dan
bradiaritmia dengan terapi bertingkat (yaitu
bradycardia pacing, overdrive
tachycardia pacing, low-energy cardioversion, dan high-energy shock defibrillation).
Terapi ICD telah menunjukkan sebagai penyelamat nyawa. Pada
studi besar, terdesain dengan baik, dan prospektif pada pasien dewasa dengan
penyakit arteri koroner dan fraksi ejeksi rendah yang bertahan dari infark
miokardial, ICD telah menunjukkan bahwa ia lebih superior dibandingkan terapi
obat antiaritmia.
Penelitian berlanjut terus dilakukan untuk menilai
besarnya manfaat terapi ICD terhadap kardiomiopati. Studi kecil pada anak-anak
dan pengalaman pribadi dan anekdotal tampaknya cenderung mendukung penggunaan
ICD pada pasien kardiomiopati hipertrofik dan aritmia, genotip malignan dari
riwayat keluarga, dan faktor lain yang mungkin dapat meningkatakan mortalitas,
dan khususnya. Risiko kematian mendadak karena aritmia.
Aktivitas pasien
Hindari kegiatan yang
membutuhkan tenaga besar atau lama. Olahraga kompetitif seharusnya tidak
diperbolehkan jika terdapat hal-hal sebagai berikut:
- Gradien outflow yang signifikan
- Aritmia ventrikular atau
supraventrikular yang signifikan
- Hipertrofi ventrikel kiri yang
signifikan
- Riwayat saudara / keluarga yang
mengalami kematian mendadak dan memiliki kardiomiopati hipertrofi
- Genotip malignan yang
teridentifikasi
- Umur muda (< 30 tahun)
- Respon tekanan darah abnormal
terhadap latihan fisik
- Adanya riwayat sinkop,
khususnya pada anak-anak
Walaupun menghindari aktivitas fisik yang intens dan
berat lebih baik dan disarankan, partisipasi dalam aktivitas olahraga rekreasi
non-kompetitif tidak dipercaya sebagai kontraindikasi.
Screening /
pemeriksaan kardiovaskular sebelum ikut serta dalam olahraga kompetitif
tampaknya dapat mengurangi frekuensi kematian mendadak tidak terduga dari HCM,
Walaupun apakah screening berskala
besar dan luas dari profesi atlet secara administratif memungkinkan atau cost-effective masih belum disepakati.
Kematian mendadak terjadi pada saat latihan fisik, tetapi
ia juga menunjukkan suatu distribusi sirkadian, dengan kebanyakan kematian pada
waktu pagi dan sore awal.
Pasien asimtomatik
Pasien kardiomiopati hipertrofik dengan jumlah yang
signifikan tidak memiliki atau menunjukkan gejala dan memiliki harapan akan
hidup yang normal, walaupun mereka seharusnya berkonsultasi untuk menghindari
kegiatan berat tertentu atau olahraga kompetitif. Pasien seharusnya menjalani pemeriksaan screening / penyaringan untuk faktor risiko dari kematian jantung
mendadak. Pada pasien dengan obstruksi outflow
yang terjadi pada waktu istirahat atau pada saat ditimbulkan, keadaan yang
menyebabkan dehidrasi atau vasodilatasi (seperti penggunaan obat vasodilator
atau obat tekanan darah diuretik ) seharusnya dihindari. Terapi reduksi
(pengurangan) septal tidak direkomendasikan pada pasien asimtomatik.
Transplantasi Jantung
Dalam kasus dimana semua bentuk penanganan pengobatan
tidak menunjukkan perbaikan, transplantasi jantung dapat menjadi suatu pilihan.
Ini juga merupakan penanganan satu-satunya untuk gagal jantung tahap akhir.
Namun demikian, transplantasi harus terjadi sebelum onset gejala-gejala seperti
hipertensi pembuluh pulmonal, malfungsi ginjal, dan tromboembolism agar menjadi
penanganan pengibatan yang sukses. Studi menunjukkan angka bertahan hidup tujuh
tahun pada 94 % pasien setelah transplantasi..
Screening (Penyaringan terduga HCM)
Walaupun HCM dapat menjadi asimtomatik, individu yang
terpengaruh dapat menunjukkan gejala yang beragam mulai dari yang ringan sampai
dengan gagal jantung yang kritis dan kematian jantung mendadak pada titik
manapun dari awal masa kanak-kanak sampai usia lanjut. HCM adalah penyebab terbanyak kematian jantung
mendadak pada atlet muda di Amerika Serikat, dan merupakan kelainan
kardiovaskulaer genetik yang paling umum. Satu studi telah menemukan bahwa
insidensi kematian jantung mendadak pada atlet muda yang kompetitif menurun
pada daerah Veneto di Italia sebanyak 89% sejak perkenalan adanya Screening
rutin kardiomiopati hipertrofik pada atlet. Namum sejak 2010, studi menunjukkan
bahwa insidensi kematian jantung mendadak, diantara semua pasien HCM, memang
menurun menjadi satu persen atau kurang.
HCM dapat dideteksi oleh ekokardiogram dengan keakuratan
80% lebih, yang dapat didahului oleh screening dengan elektrokardiogram (EKG)
untuk memeriksa abnormalitas jantung. Cardiac
magnetic resonance imaging (CMR), yang dianggap sebagai gold standard untuk menentukan gambaran
fisik komprehensif dari dinding ventrikel kiri, dapat berperan sebagai metode
screening alternatif ketika ekokardiogram memberikan hasil yag inkonklusif.
Sebagai contoh, identifikasi hipertrofi ventrikular segmental tidak bisa
dilakukan hanya dengan ekokardiografi. Dan juga, hipertrofi ventrikal kiri
dapat tidak ditemukan pada anak dibawah umur 13 tahun. Hal ini dapat mengurangi
kesahihan hasil dari ekokardiogram pasien pra-remaja. Also, left ventricular
hypertrophy may be absent in children under thirteen years of age. Namun
peneliti telah mempelajari carrier (pembawa) asimtomatik dari mutasi yang
menyebabkan HCM melalui penggunaan CMR dan telah dapat mengidentifikasi kriptus
pada jaringan septal interventrikular pada pasien ini. Telah diduga bahwa
pembentukan kriptus ini adalah indikasi dari ketidakteraturan miosit dan
dinding pembuluh yang berubah yang kemudian akan menghasilkan gambaran klinis
dari HCM. Dan yang terakhir, pengumpulan riwayat keluarga dan pemeriksaan fisik
dianggap inefektif, dan hanya memberi peringatan pada 3% pasien sebelum
kematian jantung mendadak. Kemungkinan penjelasan ini adalah bahwa pengumpulan
riwayat keluarga hanya berfokus kepada apakah ada kematian mendadak atau tidak.
Ia tidak mencantumkan usia ketika kerabat tersebut mengalami kematian jantung
mendadak, begitu juga dengan frekuensi kejadian gangguan jantung. Terlebih
lagi, dikarenakan banyak faktor yang
diperlukan untuk dipertimbangkan sebagai risiko kematian jantung mendadak, dan
tidak ada faktor yang lebih penting dari faktor lain, maka adanya ambiguitas
dalam kapan harus memberikan perlakuan khusus.
Prognosis
Laporan angka mortalitas pada pasien dengan kardiomiopati
hipertrofik antara 1% hingga 3-6%, dan studi menunjukkan bahwa secara
signifikan telah membaik sepanjang 40 tahun terakhir.
Sebuah studi yang dilakukan pada tahun 2006 melaporkan
bahwa angka kematian mendadak yang terpublikasikan sepanjang 10 tahun terakhir
lebih rendah dibandingkan angka yang dipublikasikan pada masa sebelumnya (median
1.0% (range 0.1–1.7) v 2.0% (0–3.5)). Namun demikian, HCM tetap membawa risiko
tinggi mortalitas dan morbiditas.
Satu rangkaian pasien yang terdiri dari 46 individu
dengan obstruksi midventrikular ditemukan memiliki risiko yang meningkat akan
pembentukan aneurisma apikal. Gejala dan kematian yang berhubungan dengan HCM
mirip dengan yang tidak memiliki obstruksi midventrikular ; peningkatan risiko
gejala dan kematian serupa dengan pasien yang memiliki obstruksi LVOT.
Kebanyakan pasien adalah asimtomatik. Namun disayangkan,
manifestasi klinis pertama dari penyakit ini pada individu tersebut dapat
merupakan kematian mendadak, yang kemungkinan besar dikarenakan takikardia atau
fibrilasi ventrikel. Pasien muda, khusunya anak-anak, memiliki angka mortalitas
yang lebih tinggi. Anak memiliki derajat hipertrofi ventrikel yang lebih tinggi
dan lebih simtomatik pada awal perjalanan penyakit, yang kemungkinan
dikarenakan genotip malignan muncul lebih awal dalam hidup..
Mutasi yang lebih jinak tidak mengelicit
fenotip
klinis maupun ekokardiografis atau gejala pada populasi pediatrik. Kematian
seringkali mendadak, tidak terduga, dan biasanya diasosiasikan dengan olahraga
atau latihan fisik yang berat. Diagnosis awal
merupakan langkah penting utama untuk menentukan tingkat aktivitas yang
dianggap aman.
Screening (penyaringan)
anggota keluarga derajat pertama bermanfaat untuk mengidentifikasi anggota
keluarga tambahan yang terpengaruh sebelum onset timbulnya gejala signifikan
atau kematian mendadak.
Pasien dapat memiliki serentetan aritmia, termasuk
fibrilasi atrial, flutter atrial, ektopi ventrikular, takikardia ventrikular,
dan fibrilasi ventrikular. Pasien ini termasuk diantara kelompok dengan risiko
tertinggi untuk fibrilasi ventrikel dan berpotensi dapat menimbulkan pemilihan
terapi yang sulit untuk mengurangi risiko.
Pasien memiliki kemungkinan yang tinggi akan kegagalan
jantung yang berulang yang berasal dari regurgitasi mitral dan disfungsi
diastolik yang signifikan. HCM adalah suatu kondisi progresif yang memburuk
seiring waktu, begitu juga gradien sepanjang LVOT (left ventricle outflow tract) jika dibiarkan tidak tertangani.
Fungsi sistolik biasanya terpelihara dengan baik hanya sampai tahap akhir
penyakit ini. Angina jarang pada anak-anak tapi umum ditemukan pada pasien
dewasa. Sinkop dan presinkop adalah umum ditemukan dan dapat mengidentifikasi
individu yang memiliki risiko tinggi kematian mendadak.
Edukasi Pasien
Anggota keluarga seharusnya mempelajari resusitasi
jantung-paru (RJP) / cardiopulmonary
resuscitation (CPR). Sebagai tambahan, sarankan pasien dan keluarga untuk
konseling psikososial. Edukasi agar anak dari pasien dengan kardiomiopati
hipertrofik / hypertrophic cardiomyopathy
(HCM), terutama dalam jangka umur pediatrik, untuk menjalani ekokardiografi dan
pemeriksaan genetik segera jika ekokardiogram belum mengungkap penyakit dengan jelas.
Berlakukan larangan aktivititas diantaranya penghentian
total dari aktivitas olahraga kompetitif yang tinggi dan latihan fisik yang
sangat berat, seperti mengangkat benda berat, angkat beban, dan
mencangkul.
Daftar Pustaka/Referensi
- Nasution SA. Kardiomiopati. Dalam Sudoyo AW, Setiyohadi B, Alwi I, Simadribrata MK, Setiati S, editor. Buku Ajar Ilmu Penyakit Dalam Jilid III. Jakarta: Departemen Ilmu Penyakit Dalam Fakultas Kedokteran Universitas Indonesia; 2007. p1600-1603
- Wynne J, Braunwald E. Cardiomyopathy and myocarditis. Dalam : Kasper DL et al. Harrison’s Principles of Internal Medicine 17th Edition. Inc. United States of America: The McGraw-Hill Companies; 2005.
- Maron BJ. Circulation. Contemporary Definitions and Classification of The Cardiomyopathies. New York: McGraw-Hill; 2006. p1807-1816.
- Rizzo DC. Delmar’s fundamentals of anatomy and physiology. Michigan: Biology Departement Head Professor of Biology Marygrove College Detroit; 2001. p294-311.
- Wynne J, Braunwald E. Cardiomyopathy and myocarditis. Dalam : Kasper DL et al. Harrison’s Principles of Internal Medicine 16th Edition. Inc. United States of America: The McGraw-Hill Companies; 2005.
- Gunawan CA. Kardiomiopati Hipertrofik. Cermin Dunia Kedokteran. No. 143 hal 19. 2004.
- Anonim. Profil Kesehatan Indonesia 2008. (sumber: http://www.depkes.go.id diakses 11 Desember 2015).
- Price SA dan Wilson LM. Patofisiologi, Konsep Klinis Proses-proses Penyakit, edisi 6. Jakarta: ECG; 2003. p517-529.
- Afridi HR. Imaging in Dilated Cardiomyopathy. (sumber: http://emedicine.medscape.com diakses tanggal 11 Desember 2015).
- Raphael MJ, Partridge JB. Cardiomyopathies, cardiac tumours, trauma and cardiac transplantation. Dalam. Grainger RG, Allison DJ, Adam A, Dixon AK. Diagnostic Radiology a Textbook of Medical Imaging Fourth Edition. London: Harcout Publishers Limited; 2001.
- Siregar AA. Kardiomiopati Primer pada Anak. Bagian Ilmu Kesehatan Anak Fakultas Kedokteran Universitas Sumatera Utara. (online), (http://library.usu.ac.id diakses 11 Desember 2015).
- Taylor RB. Taylor’s cardiovascular diseases: a handbook. Inc. United States of America : Springer Science; 2005.
- Rivera-Diaz, Jorge; Moosvi, Ali R. (July 1996). "Apical hypertrophic cardiomyopathy". South. Med. J. 89 (7): 711–713.
- Gersh BJ, Maron BJ, Bonow RO, et al. (December 2011). "2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: executive summary: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines". J. Thorac. Cardiovasc. Surg. 142 (6): 1303–38.
- Sherrid MV, Barac I, McKenna WJ, et al. (Apr 2005). "Multicenter study of the efficacy and safety of disopyramide in obstructive hypertrophic cardiomyopathy". J Am Coll Cardiol. 45 (8): 1251–8.
- Morrow AG (Oct 1978). "Hypertrophic subaortic stenosis. Operative methods utilized to relieve left ventricular outflow obstruction". J Thorac Cardiovasc Surg 76 (4): 423–30.
- Nakatani S, Schwammenthal E, Lever HM, Levine RA, Lytle BW, Thomas JD (Feb 1996). "New insights into the reduction of mitral valve systolic anterior motion after ventricular septal myectomy in hypertrophic obstructive cardiomyopathy". Am Heart J. 131 (2): 294–300.
- Balaram SK, Sherrid MV, Derose JJ, Hillel Z, Winson G, Swistel DG (Jul 2005). "Beyond extended myectomy for hypertrophic cardiomyopathy: the resection-plication-release (RPR) repair". Ann Thorac Surg. 80 (1): 217–23.
- McIntosh CL, Maron BJ, Cannon RO, Klues HG (Nov 1992). "Initial results of combined anterior mitral leaflet plication and ventricular septal myotomy-myectomy for relief of left ventricular outflow tract obstruction in patients with hypertrophic cardiomyopathy". Circulation 86 (5 Suppl): II60–7.
- Brilakis ES, Nishimura RA (Jul 2003). "Severe pulmonary hypertension in a patient with hypertrophic cardiomyopathy: response to alcohol septal ablation". Heart 89 (7): 790.
- Heldman AW, Wu KC, Abraham TP, Cameron DE (Jan 2007). "Myectomy or alcohol ablation surgery and percutaneous intervention go another round". J Am Coll Cardiol. 49 (3): 358–60.
- Ommen SR, Nishimura RA, Squires RW, Schaff HV, Danielson GK, Tajik AJ (Jul 1999). "Comparison of dual-chamber pacing versus septal myectomy for the treatment of patients with hypertrophic obstructive cardiomyopathy: a comparison of objective hemodynamic and exercise end points". J Am Coll Cardiol 34 (1): 191–6.
- "Autopsy reveals Foe died of heart problem", CNN.com, July 7, 2003 (retrieved November 22, 2015).Stefan Lovgren,. "Athens Olympics May Be Most Physically Demanding Ever", National Geographic, August 5, 2004 (retrieved November 22, 2015).
- Ly HQ; Greiss I; Talakic M; Guerra PG; Macle L; Thibault B; Dubuc M; Roy D, Clinical Electrophysiology Service, Department of Medicine, Montreal Heart Institute, University of Montreal, Montreal, et al. Sudden death and hypertrophic cardiomyopathy: a review. Can J Cardiol. 2005.
- Colombo MG, Botto N, Vittorini S, Paradossi U, Andreassi MG. Clinical utility of genetic tests for inherited hypertrophic and dilated cardiomyopathies. Cardiovasc Ultrasound. 2008 Dec 19. 6:62.
- Morimoto S. Sarcomeric proteins and inherited cardiomyopathies. Cardiovasc Res. 2008 Mar 1. 77(4):659-66.
- Soor GS, Luk A, Ahn E, Abraham JR, Woo A, Ralph-Edwards A, et al. Hypertrophic cardiomyopathy: current understanding and treatment objectives. J Clin Pathol. 2009 Mar. 62(3):226-35.
- Van Driest SL, Ackerman MJ, Ommen SR, Shakur R, Will ML, Nishimura RA, et al. Prevalence and severity of "benign" mutations in the beta-myosin heavy chain, cardiac troponin T, and alpha-tropomyosin genes in hypertrophic cardiomyopathy. Circulation. 2002 Dec 10. 106(24):3085-90.
- Minami Y, Kajimoto K, Terajima Y, et al. Clinical implications of midventricular obstruction in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol. 2011 Jun 7. 57(23):2346-55.
Kata Kunci Pencarian : Kardiomiopati hipertrofik, ilmu penyakit dalam, kardiologi,
artikel, makalah, tesis, desertasi, karya tulis ilmiah, jurnal, SKP (Satuan Kredit Profesi), Kompetensi, pdf, word, .pdf, .doc, .docx, skripsi,
referat, refrat, modul BBDM, Belajar Bertolak Dari Masalah, Problem Based Learning, askep (asuhan keperawatan)
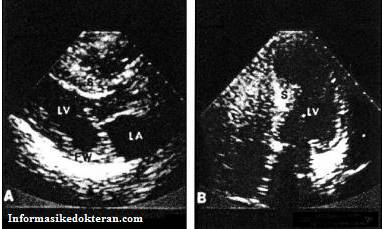


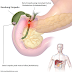




0 comments:
Posting Komentar